Terapia genica
Trattare le malattie mirando alle basi genetiche
COME FUNZIONA LA TERAPIA GENICA?
Tra le diverse terapie avanzate e di precisione, la terapia genica è una delle prime ad essere state ideate e ha l’obiettivo di trattare una patologia mirando direttamente alle sue basi genetiche. Il concetto base di questa strategia terapeutica è di fornire all’organismo una copia corretta del gene difettoso o un altro gene che possa compensarne il malfunzionamento nelle cellule colpite dalla malattia.
Esistono due principali modalità di somministrazione per la terapia genica:
- in vivo: il “gene terapeutico” viene somministrato direttamente nell’organismo del paziente, mediante un’iniezione per via locale (organo bersaglio) o per via sistemica (nella circolazione sanguigna);
- ex vivo: la correzione avviene all’esterno dell’organismo del paziente. Infatti, le cellule bersaglio vengono prelevate dal paziente, modificate geneticamente, e reintrodotte nel paziente stesso.
Per veicolare il “gene terapeutico” all’interno delle cellule o dell’organismo si utilizzano generalmente dei vettori virali: ad oggi i più utilizzati sono i vettori virali adeno-associati (AAV).
Il potenziale della terapia genica è di enorme portata poiché potrebbe rappresentare una cura per tutta una serie di gravissime malattie per cui oggi non esistono valide opzioni terapeutiche o che richiedono terapie croniche. Ad oggi la ricerca nell’ambito della terapia genica spazia dalle malattie genetiche, in particolar modo quelle rare, al cancro, passando per le malattie autoimmuni e le malattie infettive.
Il concetto di terapia genica nasce alla fine degli anni ‘80 con le nuove tecniche del DNA ricombinante che permettono di costruire pezzi di DNA contenenti sequenze geniche desiderate. Ma è solo negli ultimi anni, con il sequenziamento del genoma e l’avanzare delle biotecnologie, che si sono cominciati a vedere i primi importanti risultati nelle sperimentazioni sull’uomo e le prime terapie geniche autorizzate dall’European Medicines Agency (EMA) in Europa e della Food and Drug Administration (FDA) negli Stati Uniti. In questo ambito l’Italia ha una posizione di eccellenza a livello internazionale: sono diverse le terapie avanzate frutto di ricerche all'avanguardia "made in Italy".
La strategia è stata ideata da un team di ricercatori italiani del Tigem di Pozzuoli e testata in studi preclinici.
È impossibile non restare a bocca aperta davanti alle abili acrobazie dei jet della Pattuglia Tricolore ma è inevitabile che per il trasporto di merci siano necessari aerei di grosse dimensioni e dalla stazza mastodontica. La ricerca dell’equilibrio tra agilità e capacità di carico non ha spinto solo l’industria aeronautica sulla via del progresso ma sta guidando il cammino anche dei ricercatori che si occupano di terapia genica. Consci che i vettori virali, fondamentali per lo sviluppo di nuove terapie, debbano da una parte essere in grado di raggiungere con agilità i siti di destinazione, dall’altra essere dotati della capacità di farsi carico delle copie funzionali dei geni difettosi. E le copie - o le informazioni necessarie per assemblare le proteine mancanti - sono voluminose e richiedono spazio.
- Di: Enrico Orzes
Quali sono i problemi nella scelta degli antigeni per la realizzazione delle CAR-T da usare nei tumori solidi e quali le difficoltà e le problematiche inerenti al loro impiego contro questa classe di neoplasie? Lo spiega il prof. Ciceri dell’IRCCS Ospedale San Raffaele di Milano
Qualcuno li ha definiti i “Power Rangers” della medicina citando una serie televisiva per ragazzi in voga negli anni ’90 e forse il paragone non è poi così sbagliato se si considera che le CAR-T sono cellule immunitarie – più precisamente linfociti T – che grazie all’ingegneria genetica vengono armate con un recettore chimerico, CAR, grazie al quale possono riconoscere in maniera altamente specifica un antigene espresso dalla cellula tumorale e, in tal modo, uccidere questa cellula.
- Di: Enrico Orzes
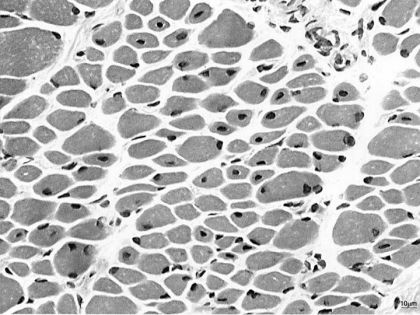
Nove bambini affetti da miopatia miotubulare legata all’X hanno avuto miglioramenti nella funzionalità neuromuscolare dopo essere stati sottoposti a terapia genica.
Negli ultimi mesi la terapia genica ha dimostrato la sua efficacia nel trattamento di diverse malattie genetiche muscolari, tra cui il più recente successo con la miopatia centronucleare (o miopatia miotubulare, MTM) legata all’X. Si tratta di una malattia neuromuscolare ereditaria con una incidenza di 1 caso ogni 50.000 nati maschi, che alla nascita presentano debolezza, ipotonia e insufficienza respiratoria gravi. Non esiste un trattamento risolutivo e, nella maggior parte dei casi, il decorso è fatale nei primi 18 mesi di vita.
- Di: Rachele Mazzaracca
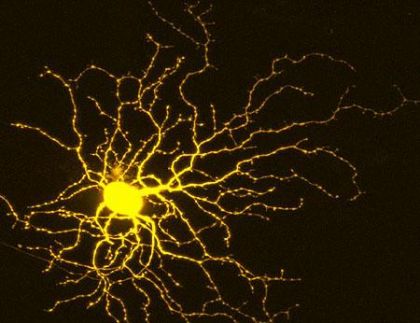
In futuro potrebbe permettere alle persone affette da degenerazione della retina di leggere e muoversi autonomamente.
Nel mondo, 36 milioni di persone soffrono di cecità completa, tanto da non poter vedere né forme né fonti di luce. Per la maggior parte di queste persone si tratterebbe di situazioni risolvibili, come ad esempio la cataratta (che diventa cecità a causa di una assistenza sanitaria inadeguata), ma spesso la cecità è dovuta a patologie che non hanno ancora una terapia approvata. Un esempio è la retinite pigmentosa, la forma più comune di cecità ereditaria, che colpisce 1,7 milioni di persone nel mondo e normalmente porta a una perdita totale della visione entro i 40 anni.
- Di: Rachele Mazzaracca
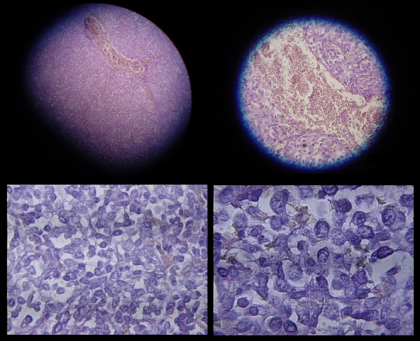
I primi risultati con le CAR-T contro i tumori solidi sono stati ottenuti su pazienti affetti da tumori cerebrali, sarcomi e mesotelioma, ma rimangono ancora dubbi ed ostacoli da superare.
Il fatto che le cellule CAR-T siano una rivoluzione nell’ambito dei trattamenti di alcuni tumori del sangue è ormai di dominio pubblico. L’approvazione, prima dall’FDA e poi dalla Commissione Europea, per Tisagenlecleucel (terapia sviluppata da Novartis) e Axicabtagene Ciloleucel (sviluppata Gilead) ha costituito il propellente necessario per sparare il razzo delle CAR-T nell’universo dei trattamenti concretamente utilizzabili per contrastare i tumori ematologici, assegnando a questa innovativa forma di terapia un ruolo di primo piano per i prossimi anni. Ma qual è, invece, la situazione sul fronte dei tumori solidi?
- Di: Enrico Orzes
All’Istituto San Raffaele-Telethon per la Terapia Genica è stato condotto uno studio clinico che ha confermato il successo di questo approccio in 8 pazienti
Sullo scacchiere delle malattie ereditarie rare la terapia genica conquista un altro territorio, quello della sindrome di Wiskott-Aldrich, allungando così l’elenco delle patologie in cui questo rivoluzionario approccio produce benefici non irrilevanti che ci avvicinano sempre più ad una possibile cura. A testimoniare questo successo è l’articolo di recente pubblicato sulla rivista Lancet Haematology riguardo ai risultati preliminari di uno studio clinico non randomizzato, in aperto, di Fase I/II nel quale sono stati arruolati 8 giovani pazienti affetti dalla sindrome di Wiskott-Aldrich ai quali è stata somministrata una innovativa terapia genica ideata per contrastare il meccanismo alla base della patologia.
- Di: Margherita De Nadai
Agenda
News da CRISPeR MANIA
a cura di Anna Meldolesi