Uno studio inglese ha messo a punto un ingegnoso sistema basato sulle cellule CAR-T la cui azione è mirata e circoscritta alle neoplasie solide. I risultati sono stati pubblicati su Cell Reports Medicine
Quando si lancia un attacco occorre conoscere il terreno su cui si muove l’esercito per evitare una facile sconfitta. Lo sapeva bene il generale cinese Sun Tzu che nel suo celebre trattato, “l’Arte della Guerra”, spiega come la conoscenza della conformazione del territorio sia un fattore di inestimabile aiuto per l’esercito in battaglia. Ugualmente bene lo sanno i ricercatori impegnati nella lotta al cancro quando approfondiscono le caratteristiche del microambiente tumorale (TME, Tumor MicroEnvironment) per far in modo che le terapie a base di cellule CAR-T colpiscano il loro obiettivo.
Il successo di terapie avanzate come le CAR-T nella lotta ai tumori ematologici è stato ormai ampiamente dimostrato ma sferrare l’attacco ai tumori solidi richiede una strategia differente. Innanzitutto, perché occorre avere accesso al microambiente tumorale che, come ormai è noto, gioca un ruolo sostanziale nella crescita del tumore e nel processo di creazione di nuove metastasi. Lo si può immaginare come uno scenario ostile, definito dalla proliferazione di vasi sanguigni (neoangiogenesi) tortuosi e inefficienti (il leakage è un fenomeno diffuso) e dalla creazione di fibroblasti associati al cancro. Alcuni ricercatori sono convinti che il microambiente tumorale possa costituire un potenziale marcatore diagnostico e prognostico e altri, come gli studiosi del team britannico, sono riusciti a sfruttarne le caratteristiche come potenziale target terapeutico.
Nel loro articolo, pubblicato ad aprile sulla rivista Cell Reports Medicine, i ricercatori descrivono un ingegnoso sistema per puntare e circoscrivere l’azione di una terapia CAR-T alle neoplasie solide, che sono generalmente caratterizzate da un ridotto apporto di ossigeno (ipossia) rispetto ai tessuti sani.
L’ipossia - ovvero la mancanza di ossigeno - è l’argomento che solo un paio d’anni fa è valso a tre scienziati - Villiam G. Kaelin Jr, Peter J. Ratcliffe e Gregg L. Semenza - il Premio Nobel per la Medicina. Durante la loro carriera essi hanno, infatti, indagato i meccanismi molecolari che le cellule mettono in atto quando si trovano in carenza di ossigeno. E per quanto riguarda i tumori, è stato osservato come la carenza di ossigeno costituisca un’opportunità per crescere e svilupparsi, evadendo le risposte del sistema immunitario. Inoltre, la ricerca condotta negli ultimi anni ha stabilito l’associazione tra ipossia e una cattiva prognosi, collegando questo parametro alla resistenza ai trattamenti (sia chemioterapici che radioterapia).
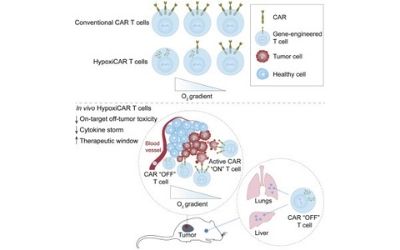
Dal momento che le terapie a base di CAR-T possono essere considerate il “potenziamento” di una specifica componente del sistema immunitario (i linfociti T per essere più precisi), i ricercatori hanno ideato il modo per dirigerle e limitarne l’azione a un sito specifico. L’interruttore di sicurezza più intuitivo e sicuro si è rivelato essere proprio l’ipossia. Il sistema, definito HypoxiCAR, si basa su CAR-T che vengono attivate solo in condizioni di ipossia - vale a dire nel microambiente di molti tumori solidi, dove le esigenze metaboliche l’alto tasso di proliferazione e una rete vascolare inefficiente riducono l’apporto di ossigeno rispetto ai tessuti sani – il che permette che la loro azione sia mirata sul bersaglio e non al di fuori del tumore.
L’efficacia dell’ingegnoso sistema è stato testato in un modello murino: le speciali CAR-T vengono infuse in topi in cui sono state precedentemente iniettate le cellule tumorali HN3, responsabili della proliferazione tumorale. I risultati mostrano che l’azione di HypoxiCAR non si è estesa ad organi sensibili, come fegato e polmone, e non si è innescata una risposta infiammatoria generalizzata. L’innovativo sistema sembra quindi in grado di prevenire la crescita tumorale e non causare gli effetti off-target che stanno rendendo così complesso l’approccio con le terapie a base di CAR-T per i tumori solidi.
Ancora una volta, i ricercatori stanno cercando una via per potenziare i trattamenti a base di CAR-T e allargare il loro raggio di azione al di fuori dai tumori ematologici. Nonostante i risultati preclinici promettenti, questo studio presenta ancora diverse limitazioni: ad esempio, non stabilisce una dose limite di CAR-T da somministrare. Ciò significa che saranno necessari maggiori approfondimenti e studi su altri modelli animali, ma se questa intuizione trovasse conferma potrebbe fornire una valida strategia per penetrare a fondo nell’ambiente selvaggio dei tumori solidi.